【药品名称】
通用名称:盐酸乌拉地尔注射液
商品名称:亚宁定®
英文名称:Urapidil Hydrochloride Injection
汉语拼音:Yan Suan Wu La Di Er Zhu She Ye
【成 份】
本品主要成份为:盐酸乌拉地尔
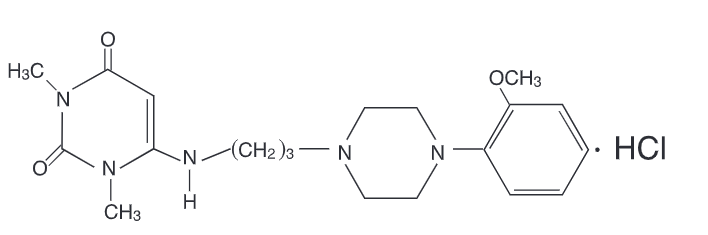
化学名称:6-{[3-[4-(2-甲氧基苯基)-1-哌嗪基]-丙基]氨基}-1,3-二甲基-2,4-(1H,3H)-嘧啶二酮
化学结构式:

分子式:C20H29N5O3·HCl
分子量:423.94
辅料名称:1,2-丙二醇,磷酸氢二钠,磷酸二氢钠,注射用水
【性 状】
无色澄明液体
【适应症】
- 用于治疗高血压危象(如血压急剧升高),重度和极重度高血压以及难治性高血压。
- 用于控制围手术期高血压。
【规 格】
5ml:25mg
每支(5ml)注射液含27.35mg盐酸乌拉地尔(相当于25mg乌拉地尔)。
【用法用量】
1. 治疗高血压危象、重度和极重度高血压,以及难治性高血压的给药方法: 1) 静脉注射 缓慢静注10-50mg乌拉地尔,监测血压变化,降压效果通常在5分钟内显示。若效果不够满意,可重复用药。
2) 持续静脉点滴或使用输液泵本品在静脉注射后,为了维持其降压效果,可持续静脉点滴,液体按下述方法配制:通常将250mg乌拉地尔(相当于10支25mg盐酸乌拉地尔注射液)加入到静脉输液中,如生理盐水、5%或10%的葡萄糖。如果使用输液泵,可将20ml注射液(=100mg乌拉地尔)注入到输液泵中,再将上述液体稀释到50ml。静脉输液的最大药物浓度为每毫升4mg乌拉地尔。 输入速度根据病人的血压酌情调整,初始输入速度可达2mg/min,维持给药的速度为9mg/h。(若将250mg乌拉地尔溶解在500ml液体中,则1mg乌拉地尔相当于44滴或2.2ml输入液)。
2. 围手术期高血压的给药方法
本品单次、重复静脉注射及长时间静脉输入均可,亦可在静脉注射后持续静脉输入以维持血压的稳定。静脉给药时患者应取卧位。从毒理学方面考虑治疗时间一般不超过7天。
配伍禁忌 本品不能与碱性液体混合,因其酸性性质可能引起溶液混浊或絮状物形成。
【不良反应】 使用本品后,病人可能出现下列不良反应:血管性水肿、荨麻疹、鼻塞、阴茎异常勃起、头痛、头晕、恶心、呕吐、出汗、烦躁、乏力、心悸、心律不齐、心动过速或过缓、呼吸困难、上胸部压迫感或疼痛等症状,其原因多为血压降得太快所致,通常在数分钟内即可消失,一般无须中断治疗。偶见因变换姿势而造成的血压下降。过敏反应(如瘙痒,皮肤发红,皮疹等)少见。极个别病例在口服本药时出现血小板计数减少,但血清免疫学研究尚未证实其因果关系。
【禁 忌】 禁用于对本品中成份过敏的患者。 主动脉峡部狭窄或动静脉分流的患者禁用(肾透析时的分流除外)。 哺乳期妇女禁用。
【注意事项】 下列情况使用本品时需要特别注意:
- 机械功能障碍引起的心力衰竭,例如大动脉或者二尖瓣狭窄、肺栓塞或者由于心包疾病引起的心功能损害;
- 儿童,因为无相关研究;
- 肝功能障碍患者;
- 中度到重度肾功能不全患者;
- 老年患者;
- 合用西咪替丁的患者(参见【药物相互作用】)。
另外乌拉地尔可能会影响驾驶或操作机器的能力。如果本品不是最先使用的降压药,那么在使用本品之前应间隔充分的时间,使先服用的其他降压药显示效应,必要时应适当减少本品的剂量。血压骤然下降可能引起心动过缓甚至心脏停搏。使用本品疗程一般不超过7天。已经证实,配制好的溶液化学和物理稳定性为15-25°C时50小时。从微生物学角度来看,配制好的溶液应立即使用。如果不能立即使用,使用者应对贮存的时间和条件负责。
【孕妇及哺乳期妇女用药】
哺乳期妇女禁用。对于孕妇,仅在绝对必要的情况下方可使用本品。目前尚无资料说明本品在妊娠期前6个月使用的安全性,妊娠期后三个月使用的资料亦很有限。
【儿童用药】
儿童很少使用本药,目前尚缺乏这方面的资料。
【老年用药】
老年患者须谨慎使用降压药,且初始剂量宜小,因为他们对药物的敏感性有时难以估计。
【药物相互作用】
若患者同时使用α受体阻断剂、血管舒张剂或其他抗高血压药物;饮酒或病人存在血容量不足的情况(如腹泻、呕吐),可增强本品的降压作用。同时使用西咪替丁可使本品的血药浓度上升,最高达15%。由于目前还没有足够的与ACE抑制剂合用的信息,所以目前暂不推荐这种联合疗法。
【药物过量】
药物过量的症状包括:
- 循环系统症状:头晕、直立性低血压、虚脱
- 中枢神经系统症状:疲劳、反应迟钝
药物过量的治疗:
发生严重低血压可抬高下肢,补充血容量。如果无效,可缓慢静脉注射缩血管药物,不断监测血压变化。极少数病例需给予儿茶酚胺(例如肾上腺素0.5-1.0mg,用等渗氯化钠溶液稀释至10ml)。
【药理毒理】
药理作用 盐酸乌拉地尔具有中枢和外周双重的作用机制。在外周,它可阻断突触后α1受体、抑制儿茶酚胺的缩血管作用,从而降低外周血管阻力和心脏负荷;在中枢,通过兴奋5-羟色胺-1A受体,调整循环中枢的活性,防止因交感反射引起的血压升高及心率加快。毒理研究 急性毒性研究表明:动物(小鼠、大鼠、兔、狗)应用本品后的LD50与人类每日治疗剂量之比,在静脉注射后为70-180倍;在静脉点滴后为100-840倍;口服给药后为610-870倍。慢性毒性研究未发现致畸、致癌及致突变作用。通过对大鼠和小鼠所做的实验表明,本品可提高动物催乳素的水平,刺激乳房组织的生长。但人类使用推荐的治疗剂量后无上述效应。根据药物作用机制的研究,本品不会使人类激素调节异常。
【药代动力学】
静脉注射乌拉地尔后,在体内分布呈二室模型,分布相半衰期约为35分钟。分布容积0.8(0.6-1.2)L/Kg。血浆清除半衰期为2.7(1.8-3.9)小时,蛋白结合率80%。50-70%的乌拉地尔通过肾脏排泄,其余由胆道排出。排泄物中约10%为药物原形,其余为代谢产物。主要代谢物为无抗高血压活性的药物羟化形式。
【贮 藏】
本品应在25°C以下保存。
不要使用过期的药物。药品放在儿童够不到的地方。
【包 装】
安瓿,5支/盒
【有效期】
24个月
【执行标准】
进口药品注册标准:JX20160055
【批准文号】
进口药品注册证号:H20160363
【生产企业】
企业名称:Takeda GmbH
地 址:
Byk-Gulden-Straβe 2
78467 Konstanz
Germany
邮政编码:78467
电话号码:+49-7531-84-0
传真号码:+49-7531-84-2474
网 址:http://www.takeda.com
生产地址:
Takeda Austria GmbH
St. Peter-Str. 25
AT-4020 Linz
Austria